Contexte
L'efficacité du textile à créer une barrière contre la pénétration/prolifération de micro-organismes est un paramètre essentiel des vêtements de protection médicaux ou de la literie hospitalière. Récemment, on a pu constater un progrès important dans le développement de matériaux et de procédures textiles destinés à protéger les personnes contre plusieurs agents pathogènes.
Dans un milieu hospitalier il est nécessaire de sélectionner des textiles appropriés créant une barrière efficace contre la pénétration ou le transfert de micro-organismes à l'état humide et à sec.
Dans le cas d'émergences, telles que les épidémies de SARS ou d’Ebola et plus récemment du virus corona, les propriétés barrières sauvent des vies.
Centexbel dispose de l'expertise et des équipements pour évaluer les propriétés barrières de textiles, casaques, masques et draps chirurgiens contre les micro-organismes et le sang.
Résistance à la pénétration d'agents pathogènes
Normes
ISO 16604: resistance to penetration by contaminated liquid under hydrostatic pressure (ISO 16603 synthetic blood test –screening)
ISO 22610: resistance to penetration by infective agents due to mechanical contact with substances containing contaminated liquids
ISO/DIS 22611: resistance to penetration by contaminated liquid aerosols
ISO 22612: resistance to penetration by contaminated solid particles
Résultats
Classification des niveaux de prestation
Résistance à la pénétration d'agents pathogènes sous pression hydrostatique
Normes
ISO 16603 : synthetic blood resistance penetration
Résultats
Pass/fail
Pressions successives
- 0, 1.75, 3.5, 7, 14 and 20 kPa (5’)
- 0 kPa 5’-14 kPa 1’-0 kPa 4’
Cette méthode d'essai est basée sur ASTM F1670
Pénétration bactérienne à l'état humide
Le Règlement Européen relatif aux dispositifs médicaux met la responsabilité pour éviter les infections provoquées par les dispositifs sur le producteur. Dans le but de faire preuve de la conformité avec ce règlement et de donner une descirption du produit à l'utilisateur, il est nécessaire d'utiliser des méthodes d'essai harmonisées et reconnues de manière internationale.
La méthode d'essai ci-dessous se base sur des techniques microbiologiques et par conséquent elle est destinée à être effectuée exclusivement par des labos qui ont l'expérience et les équipements appropriés.
Normes
ISO 22610: Champs chirurgicaux, casaques et tenues de bloc, utilisés en tant que dispositifs médicaux, pour les patients, le personnel et les équipements — Méthode d'essai de résistance à la pénétration de la barrière bactérienne à l'état humide
Principe
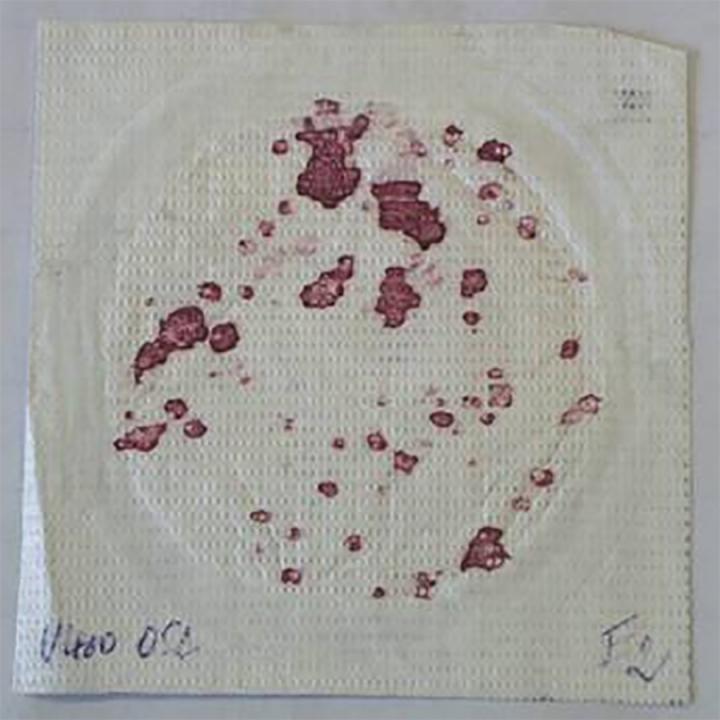
A sheet of donor material, of the same size as the test specimen and carrying the bacteria, is placed on the test specimen with the contaminated side facing down and covered by a sheet of HDPE cover film.
Two conical metal rings, close-fitting into each other, hold the three sheets together. The assemblage of materials is placed on an agar plate with the steel rings hanging freely outside the brim, applying a tensile force. An abrasion-resistant finger is placed on top of the materials with a specified force to bring the test specimen into contact with the agar surface. The finger is moved over the entire surface of the plate in less than 15 minutes by means of a pivoted lever moved by an eccentric cam. The assemblage of materials, stretched by the weight of the steel rings, ensures that only a small area of the test specimen is brought into contact with the agar surface at any given time. Due to the combined effect of rubbing and liquid migration up from the agar surface, bacteria may pass from the donor material through the test specimen down to the agar surface.
The test is carried out for 15 minutes. After 15 minutes the agar plate is replaced by a fresh one, and the test is repeated with the same assemblage, i.e. the same donor and test specimen. Five consecutive tests are performed with the same assemblage enabling an estimation of the penetration over time.
An estimation of the bacterial contamination on the upper side of the test specimen and the bacterial load remaining on the donor material may be determined by using the same technique
Envoyez vos échantillons à
Centexbel - Labo Micriobiologique
Rue du Travail 5
4460 Grâce-Hollogne
Belgium
+32 4 296 82 00
g-h@centexbel.be